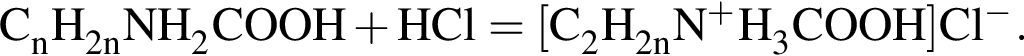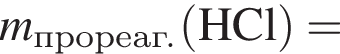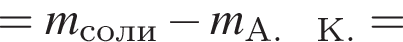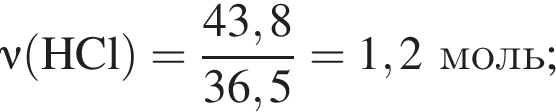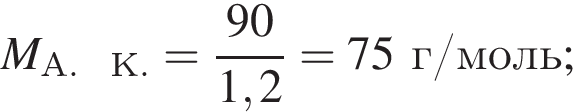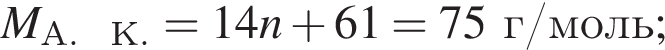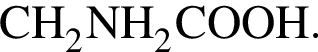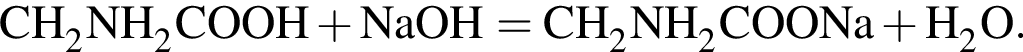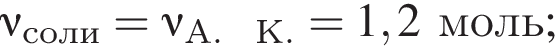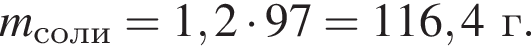Задание № 1968 
Сложность: III
Расчетные задачи в органической химии
i
Порцию природной аминокислоты массой 180 г разделили на две равные части. Одну часть обработали избытком хлороводорода, в результате чего образовалась соль массой 133,8 г. Вторую часть обработали избытком водного раствора гидроксида натрия. Найдите массу (г) образовавшейся при этом соли.
Решение. Дальнейшие расчёты будут строиться на том, что в природной аминокислоте содержатся одна аминогруппа и одна карбоксильная группа.
1. Составим уравнение первой реакции:
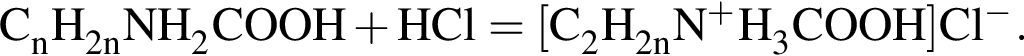
2. Так как изначальную порцию аминокислоты разделили на две равные по массе порции, то прореагировало 90 г аминокислоты (хлороводород в избытке). Чтобы в итоге вычислить количество вещества аминокислоты, надо сначала найти массу прореагировавшего хлороводорода. По закону действующих масс имеем (А. К. = аминокислота):


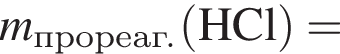
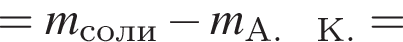

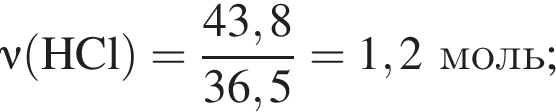
Из уравнения реакции:

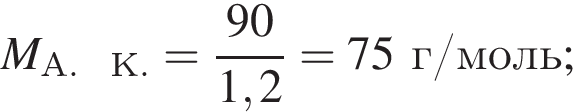
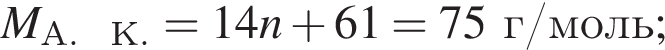

Формула кислоты: 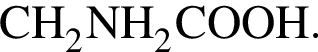
3. Составим уравнение второй реакции:
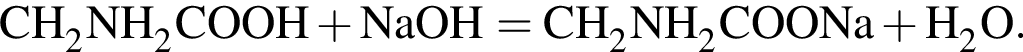
4. Найдём массу получившейся натриевой соли:
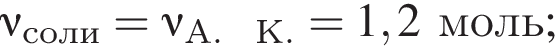
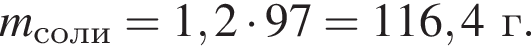
Ответ: 116.
Ответ: 116